- 1. ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ (Chemical Reactions and Equations)
- 2. এছিড, ক্ষাৰক আৰু লৱণ (Acids, Bases, and Salts)
- 3. ধাতু আৰু অধাতু (Metals and Non-metals)
- 4. কাৰ্বন আৰু তাৰ যৌগ (Carbon and Its Compounds)
- 5. মৌলৰ পৰ্যাবৃত্ত শ্ৰেণীবিভাজন (Periodic Classification of Elements)
- 6. জীৱন প্ৰক্ৰিয়া (Life Processes)
- 7. নিয়ন্ত্ৰণ আৰু সমন্বয় (Control and Coordination)
- 8. জীৱই কেনেকৈ বংশবিস্তাৰ কৰে? (How Do Organisms Reproduce?)
- 9. বংশগতি আৰু ক্ৰমবিকাশ (Heredity and Evolution)
- 10. পোহৰ- প্ৰতিফলন আৰু প্ৰতিসৰণ (Light – Reflection and Refraction)
- 11. মানুহৰ চকু আৰু বাৰেবৰণীয়া পৃথিৱী (The Human Eye and the Colourful World)
- 12. বিদ্যুত (Electricity)
- 13. বিদ্যুত - প্ৰবাহৰ চুম্বকীয় ক্ৰিয়া (Magnetic Effects of Electric Current)
- 14. শক্তিৰ উৎসসমূহ (Sources of Energy)
- 15. আমাৰ পৰিবেশ (Our Environment)
- 16. প্রাকৃতিক সম্পদৰ ব্যৱস্থাপনা (Management of Natural Resources)
SEBA Class 10 Science Chapter 4 Question Answers – কাৰ্বন আৰু তাৰ যৌগ (Carbon and Its Compounds) | Assamese Medium
Class 10 Science Chapter 4 - Carbon and Its Compounds Solutions
তলত Class 10 Science ৰ Chapter 4 Carbon and Its Compounds (কাৰ্বন আৰু তাৰ যৌগ) ৰ Questions Answers সমূহ সুন্দৰকৈ আগবঢ়োৱা হৈছে। Prepare for HSLC 2025 with SEBA Class 10 Science Chapter 4 – Carbon and Its Compounds (কাৰ্বন আৰু তাৰ যৌগ). Our Assamese notes provide clear question answers and explanations based on the latest pattern. Understand bonding, reactions, and properties in Chapter 4 Science Carbon and Its Compounds easily. Explore topics like electron dot structures, homologous series, and covalent bonding with our detailed SEBA Class 10 Science Chapter 4 notes in Assamese Medium. Revise fast and score better with our trusted Chapter 4 Science Carbon and Its Compounds guide made for SEBA students.
Chapter 4: কাৰ্বন আৰু তাৰ যৌগ - প্রশ্নোত্তৰ
Table of Contents
প্রশ্নাৱলী (পৃষ্ঠা ৬১)
উত্তৰ: কাৰ্বন ডাই অক্সাইড (CO₂)ত এটা কাৰ্বন পৰমাণু আৰু দুটা অক্সিজেন পৰমাণু থাকে। কাৰ্বনৰ যোজ্যতা ৪ আৰু অক্সিজেনৰ যোজ্যতা ২। কাৰ্বনে প্ৰতিটো অক্সিজেনৰ সৈতে দুটা ইলেক্ট্ৰন ভাগ-বতৰা কৰি দ্বি-সহযোজী বান্ধনি গঠন কৰে।
ইলেক্ট্ৰন বিন্দু গঠন:
ইলেক্ট্ৰন বিন্দু গঠন:

উত্তৰ: আঠটা ছালফাৰ পৰমাণুৰে গঠিত অণু হ’ল S₈, যিটো এটা বলয় আকৃতিৰ অণু। ছালফাৰৰ যোজ্যতা ২, গতিকে প্ৰতিটো ছালফাৰ পৰমাণুৱে দুটা পৰমাণুৰ সৈতে এডাল এডাল সহযোজী বান্ধনি গঠন কৰি বলয়াকাৰ ছালফাৰ অণু গঠন কৰে।
ইলেক্ট্ৰন বিন্দু গঠন:

প্রশ্নাৱলী (পৃষ্ঠা ৬৮-৬৯)
উত্তৰ: পেন্টেনৰ আণৱিক সংকেত C₅H₁₂। ইয়াৰ তিনিটা গঠন সমযোজী সম্ভৱ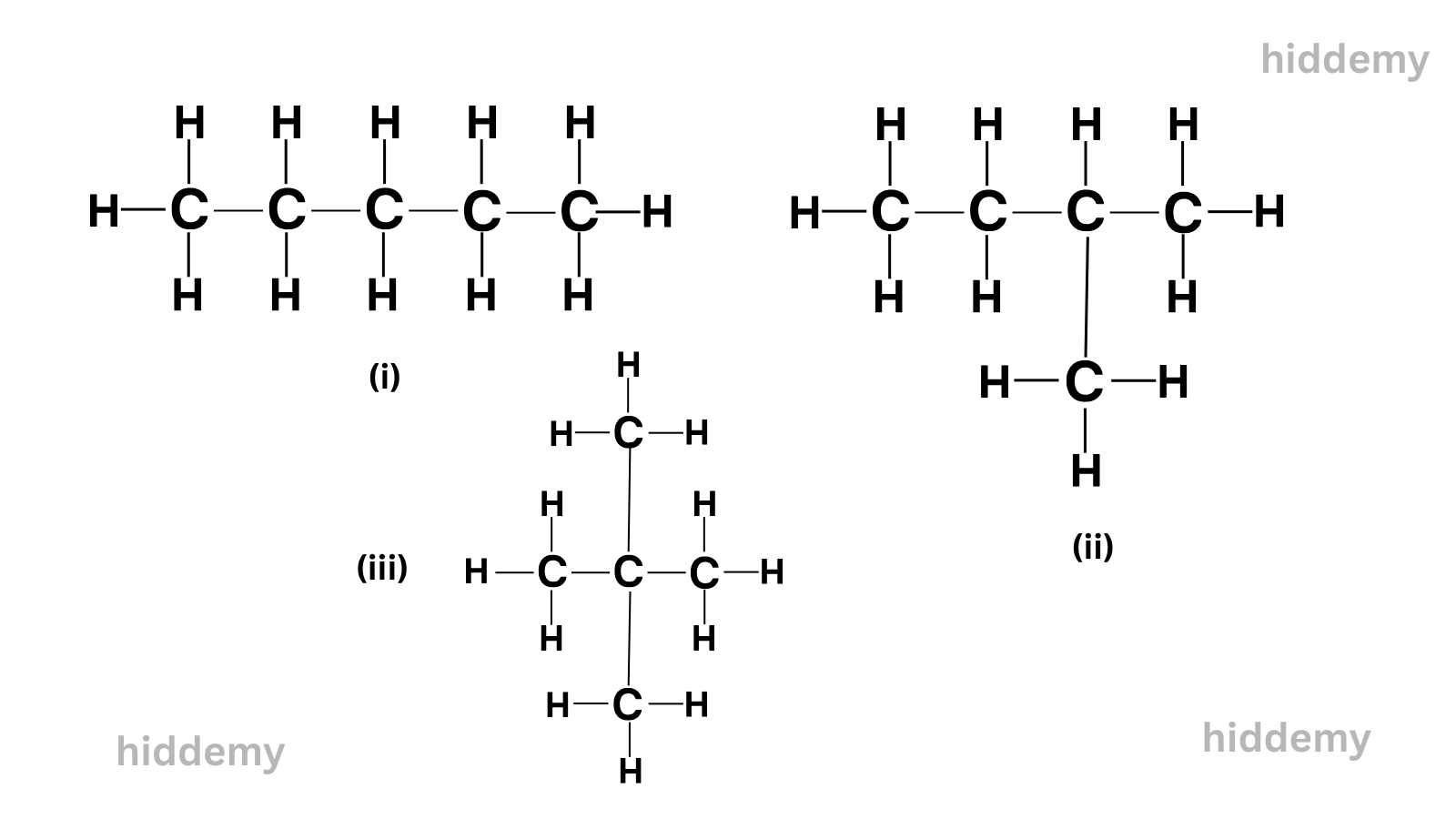
মুঠ সমযোজী: তিনিটা।
উত্তৰ:
কাৰ্বনৰ দুটা প্ৰধান ধৰ্ম:
- কেটিনেচন (Catenation): কাৰ্বনে নিজৰ সৈতে বান্ধনি গঠন কৰি দীঘল শৃংখল, শাখাযুক্ত শৃংখল বা চক্ৰীয় শৃংখল গঠন কৰিব পাৰে। যাৰ ফলত বিভিন্ন যৌগ গঠন সম্ভৱপৰ হয়।
- চতুৰ্সহযোজী (Tetravalency): কাৰ্বনৰ যোজ্যতা 4, গতিকে ই 4টা কাৰ্বন বা অন্য মৌলৰ (যেনে H, O, N) সৈতে ল'গ লাগি সহযোজী বান্ধনি গঠন কৰিব পাৰে। কাৰ্বনৰ এই বৈশিষ্ট্যৰ বাবে বিভিন্ন ধৰণৰ যৌগ গঠন সম্ভৱ হয়।
উত্তৰ: চাইক্ল’পেন্টেনৰ আণৱিক সংকেত C₅H₁₀। ই এটা চক্ৰীয় হাইড্ৰ’কাৰ্বন, য’ত ৫টা কাৰ্বন পৰমাণুৱে বলয় গঠন কৰে, আৰু প্ৰতিটো কাৰ্বনৰ সৈতে ২টা হাইড্ৰ’জেন সংযুক্ত হৈ থাকে।
গঠন:

i. ইথানয়িক এচিড (CH₃COOH):
নাম: ইথানয়িক এচিড। ই এটা কাৰ্বক্সিলিক এচিড।

ii. বিউটান’ন (CH₃COCH₂CH₃):
নাম: বিউটেন-২-অ’ন। ই এটা কিট’ন, য’ত কাৰ্বন শৃংখলত ৪টা কাৰ্বন আৰু এটা কিট’ন কাৰ্যকৰীমূলক (-CO-) থাকে।

iii. ব্ৰ’ম’পেন্টেন (CH₂Br-CH₂-CH₂-CH₂-CH₃):
নাম: ১-ব্ৰ’ম’পেন্টেন। ই এটা এলকেনৰ প্ৰতিস্থাপিত যৌগ, য’ত পেন্টেন শৃংখলৰ প্ৰথম কাৰ্বনত ব্ৰ’মিন সংযুক্ত হৈ আছে।

iv. হেক্সানেল (CH₃─CH₂─CH₂─CH₂─CH₂─CHO):
ই এটা এলডিহাইড, য’ত ৬টা কাৰ্বনৰ শৃংখলত এলডিহাইড কাৰ্যকৰীমূলক (-CHO) থাকে।

উত্তৰ: হয়, ব্ৰ’ম’পেন্টেনৰ গঠন সমযোজী সম্ভৱ।
ব্ৰ’ম’পেন্টেনৰ সংকেত: C₅H₁₁Br।
সমযোজীৰ উদাহৰণ:
- ১-ব্ৰ’ম’পেন্টেন: CH₂Br-CH₂-CH₂-CH₂-CH₃
- ২-ব্ৰ’ম’পেন্টেন: CH₃-CHBr-CH₂-CH₂-CH₃
- ৩-ব্ৰ’ম’পেন্টেন: CH₃-CH₂-CHBr-CH₂-CH₃
ব্ৰ’মিন পৰমাণুৰ অৱস্থানৰ ওপৰত নিৰ্ভৰ কৰি বিভিন্ন গঠন সম্ভৱ।
CH₃-CH₂Br:
- ব্ৰ'মো ইথেন/ ইথাইল ব্ৰ'মাইড
HCHO:
- মিথানেল
CH≡C-CH₂-CH₂-CH₂-CH₃:
- হেক্সাইন
প্রশ্নাৱলী (পৃষ্ঠা ৭১)
উত্তৰ: ইথানল (C₂H₅OH)ক ইথানয়িক এচিড (CH₃COOH)লৈ ৰূপান্তৰ কৰিলে অক্সিজেন যোগ হয় আৰু হাইড্ৰ’জেন হেৰুৱাই, যিটো জাৰণ বিক্ৰিয়াৰ বৈশিষ্ট্য। সেয়েহে ইথানলক ইথানয়িক এচিডলৈ ৰূপান্তৰ কৰাটো এটা জাৰণ বিক্ৰিয়া।
বিক্ৰিয়া:
C₂H₅OH → CH₃COOH
(জাৰক পদাৰ্থ যেনে ক্ষাৰকীয় পটাছিয়াম পাৰমেঙ্গানেট বা আম্লিক পটাছিয়াম ডাইক্ৰ’মেটৰ উপস্থিতিত।)
উত্তৰ: লোহা জোৰা দিয়াৰ সময়ত ইথাইন (C₂H₂)ৰ সৈতে কেৱল অক্সিজেন ব্যৱহাৰ কৰা হয় কাৰণ বিশুদ্ধ অক্সিজেনে ইথাইনৰ সম্পূৰ্ণ দহন ঘটায়, যাৰ ফলত অতি উচ্চ তাপ (প্ৰায় ৩০০০°C) উৎপন্ন হয়, যিটো লোহা গলোৱাৰ বাবে অতি প্ৰয়োজন।
আনহাতে ইথাইনৰ লগত বায়ু ব্যৱহাৰ কৰা নহয় কাৰণ বায়ুত অক্সিজেনৰ পৰিমাণ মাত্ৰ ২০%, বাকী অংশ নাইট্ৰ’জেন আৰু অন্যান্য গেছ। বায়ু ব্যৱহাৰ কৰিলে দহন অসম্পূৰ্ণ হ’ব আৰু কম পৰিমাণৰ তাপ উৎপন্ন হ’ব, যিটো ঢালাইৰ বাবে অপৰ্যাপ্ত।
প্রশ্নাৱলী (পৃষ্ঠা ৭৪)
উত্তৰ: এলক’হল (যেনে ইথানল) আৰু কাৰ্বক্সিলিক এচিড (যেনে ইথানয়িক এচিড)ৰ মাজৰ প্ৰভেদ দেখুৱাবলৈ তলত দিয়া পৰীক্ষাটো কৰিব পাৰি:
পৰীক্ষা: ছডিয়াম বাইকাৰ্বনেট (NaHCO₃) পৰীক্ষা-
পদ্ধতি: দুটা পৰীক্ষা নলীত ক্ৰমে ইথানল আৰু ইথানয়িক এচিড লৈ তাত অলপ ছডিয়াম বাইকাৰ্বনেট যোগ কৰিব লাগিব।
পৰ্যবেক্ষণ:
- ইথানয়িক এচিডৰ নলীত ফচফচ শব্দৰ সৈতে বুদবুদ উৎপন্ন হ’ব আৰু কাৰ্বন ডাই অক্সাইড (CO₂) গেছ নিৰ্গত হ’ব। এই গেছক চূণপানীৰ মাজেৰে পঠিয়ালে চূণপানী ঘোলা হ’ব।
- আনহাতে, ইথানলৰ নলীত কোনো বিক্ৰিয়া সংঘটিত নহ’ব, কাৰণ ইথানলে ছডিয়াম বাইকাৰ্বনেটৰ সৈতে বিক্ৰিয়া নকৰে।
সমীকৰণ:
CH₃COOH + NaHCO₃ → CH₃COONa + H₂O + CO₂
ব্যাখ্যা: কাৰ্বক্সিলিক এচিডৰ আম্লিক ধৰ্মৰ বাবে ই কাৰ্বনেটৰ সৈতে বিক্ৰিয়া কৰি CO₂ উৎপন্ন কৰে, কিন্তু এলক’হলৰ এনে ধৰ্ম নাই।
উত্তৰ: জাৰক দ্ৰৱ্য হ’ল এনে পদাৰ্থ যিয়ে অন্য পদাৰ্থৰ জাৰণ ঘটায়, আৰু নিজে বিজাৰিত হয়। অৰ্থাৎ জাৰক পদাৰ্থই অন্য পদাৰ্থক অক্সিজেন যোগান ধৰে।
উদাহৰণ: ক্ষাৰকীয় পটাছিয়াম পাৰমেঙ্গানেট (KMnO₄), আম্লিক পটাছিয়াম ডাইক্ৰ’মেট (K₂Cr₂O₇), নাইট্ৰিক এচিড (HNO₃)।
ইথানলক ইথানয়িক এচিডলৈ জাৰণ ঘটাবলৈ KMnO₄ ব্যৱহাৰ কৰা হয়।
প্রশ্নাৱলী (পৃষ্ঠা ৬৮-৬৯, অতিৰিক্ত প্ৰশ্ন)
উত্তৰ: হয়, অপমাৰ্জক ব্যৱহাৰ কৰি পানী কঠিন হয় নে নহয় ক’ব পাৰি।
পদ্ধতি: পানীত অলপ অপমাৰ্জক (যেনে ডিটাৰজেণ্ট) যোগ কৰি ভালদৰে জোকাৰি দিলে ফেন উৎপন্ন হ’ব।
- যদি পানীত সহজে ফেন উৎপন্ন হয়, তেন্তে সেই পানী কোমল।
- যদি ফেন কমকৈ উৎপন্ন হয় বা গেদৰ দৰে পদাৰ্থ জমা হয়, তেন্তে সেই পানী কঠিন হ’ব। কিন্তু অপমাৰ্জক সাধাৰণতে কঠিন পানীতো কাৰ্যক্ষম হৈ পৰে।
ব্যাখ্যা: কঠিন পানীত কেলছিয়াম (Ca²⁺) আৰু মেগনেছিয়াম (Mg²⁺) আয়ন থাকে। চাবোনে এই আয়নৰ সৈতে অদ্ৰৱণীয় গেদ গঠন কৰে, কিন্তু অপমাৰ্জকে এনে গেদ গঠন নকৰে। তথাপিও ফেনৰ পৰিমাণৰ ওপৰত নিৰ্ভৰ কৰি পানীৰ প্ৰকৃতি বুজিব পাৰি।
উত্তৰ: কাপোৰ পৰিষ্কাৰ কৰিবলৈ জোকাৰিব লাগে কাৰণ:
- চাবোন বা অপমাৰ্জকে পানীত মাইছেল গঠন কৰে, য’ত জলবিকৰ্ষী পুচ্ছই মলি বা তেলৰ টোপালৰ সৈতে সংযুক্ত হয় আৰু জলাকৰ্ষী মূৰ পানীৰ সৈতে সংযুক্ত হৈ থাকে।
- জোকাৰিলে এই মাইছেলবোৰে মলি বা তেলৰ টোপালক কাপোৰৰ পৰা আঁতৰাই পানীত ইমালছন গঠন কৰে, যিটো ধুই পেলোৱা হয়।
- লগতে জোকাৰিলে যান্ত্ৰিক শক্তিয়ে মলিৰ কণাবোৰক কাপোৰৰ আঁহৰ মাজৰ পৰা আঁতৰোৱাত সহায় কৰে যাৰ ফলত কাপোৰ পৰিষ্কাৰ হয়।
অনুশীলনী
(a) ৬টা সহযোজী বান্ধনি আছে।
(b) ৭টা সহযোজী বান্ধনি আছে।
(c) ৪টা সহযোজী বান্ধনি আছে।
(d) ৯টা সহযোজী বান্ধনি আছে।
উত্তৰ: (b) ৭টা সহযোজী বান্ধনি আছে।
ব্যাখ্যা:
ইথেনৰ সংকেত C₂H₆। গঠন: CH₃-CH₃।
দুটা কাৰ্বনৰ মাজত এডাল সহযোজী আছে।
লগতে প্ৰতিটো কাৰ্বনৰ সৈতে ৩টা হাইড্ৰ’জেন সংযুক্ত হৈ আছে, অৰ্থাৎ ৬ ডাল C-H বান্ধনি আছে।
মুঠ: ১ + ৬ = ৭টা সহযোজী বান্ধনি।
(a) কাৰ্বক্সিলিক এচিড
(b) এলডিহাইড
(c) কিট’ন
(d) এলক’হল
উত্তৰ: (c) কিট’ন
ব্যাখ্যা:
বিউটান’ন (CH₃COCH₂CH₃), য’ত কাৰ্যকৰীমূলক হ’ল -CO- (কিট’ন মূলক)।
(a) খাদ্য ভালদৰে নিসিজিল।
(b) ইন্ধন সম্পূৰ্ণৰূপে দহন নহয়।
(c) ইন্ধনটো সিক্ত।
(d) ইন্ধনটো সম্পূৰ্ণকৈ দহন হয়।
উত্তৰ: (b) ইন্ধন সম্পূৰ্ণৰূপে দহন নহয়।
ব্যাখ্যা:
ৰন্ধনত ব্যৱহৃত বৰ্তনৰ তলফালে ক’লা পৰে কাৰণ ব্যৱহৃত ইন্ধন (যেনে কেৰাচিন, LPG) অপৰ্যাপ্ত অক্সিজেনৰ উপস্থিতিত অসম্পূৰ্ণ দহন ঘটে। এনে দহনত কাৰ্বন কণা (কাজল) উৎপন্ন হয়, যি বৰ্তনৰ তলিত জমা হয়।
উত্তৰ: CHCl₃ হ’ল ক্ল’ৰ’ফৰ্ম। ইয়াত এটা কাৰ্বন, এটা হাইড্ৰ’জেন, আৰু তিনিটা ক্ল’ৰিন পৰমাণু থাকে।
সহযোজী বান্ধনিৰ স্বৰূপ:
কাৰ্বনে ৪টা ইলেক্ট্ৰন ভাগ-বতৰা কৰি ৪টা একক সহযোজী বান্ধনি গঠন কৰে। অৰ্থাৎ ১টা Hৰ সৈতে C-H আৰু ৩টা Clৰ সৈতে C-Cl বান্ধনি গঠন কৰে।
এই বান্ধনিবোৰ সহযোজী বান্ধনি কাৰণ ইহঁতে ইলেক্ট্ৰন ভাগ-বতৰা কৰি গঠিত হয়।
গঠন: CHCl₃
a. ইথানয়িক এচিড (CH₃COOH):
গঠন: CH₃-C(=O)-OH
ইলেক্ট্ৰন বিন্দু গঠন:
b. H₂S:
ছালফাৰৰ যোজ্যতা ২, ২টা Hৰ সৈতে একক বান্ধনি গঠন কৰে।
ইলেক্ট্ৰন বিন্দু গঠন:
c. প্ৰ’পান’ন (CH₃COCH₃):
গঠন: CH₃-C(=O)-CH₃
ইলেক্ট্ৰন বিন্দু গঠন:
d. F₂:
ইলেক্ট্ৰন বিন্দু গঠন:
উত্তৰ: যিবোৰ শ্ৰেণীৰ যৌগত একে কাৰ্যকৰীমূলক থাকে আৰু প্ৰতিটো অনুক্ৰমিক যৌগৰ মাজত -CH₂ মূলকৰ পাৰ্থক্য থাকে, তাকে সমগণীয় শ্ৰেণী বোলে।
বৈশিষ্ট্য:
- সমগণবিলাকৰ ৰাসায়নিক ধৰ্ম প্ৰায় একে।
- ভৌতিক ধৰ্ম (যেনে গলনাংক, উতলাংক) আণৱিক ভৰৰ সৈতে ক্ৰমিকভাৱে সলনি হয়।
উদাহৰণ: এলক’হল শ্ৰেণী
- CH₃OH (মিথান’ল)
- C₂H₅OH (ইথান’ল)
- C₃H₇OH (প্ৰ’পান’ল)
- C₄H₉OH (বিউটান’ল)
এই যৌগবোৰৰ কাৰ্যকৰীমূলক -OH (এলক’হল), আৰু প্ৰতিটো সমগণ (CH₃, C₂H₅)ৰ মাজত -CH₂ মূলকৰ পাৰ্থক্য আছে।
উত্তৰ:
ভৌতিক ধৰ্ম:
| ইথানল (C₂H₅OH) | ইথানয়িক এচিড (CH₃COOH) | |
|---|---|---|
| গোন্ধ | সুখদায়ক, মিঠা গোন্ধযুক্ত। | টেঙা, তীব্ৰ, উগ্ৰ গোন্ধযুক্ত (ভিনেগাৰৰ দৰে)। |
| দ্ৰৱণীয়তা | পানীত সম্পূৰ্ণৰূপে দ্ৰৱণীয়। | পানীত সম্পূৰ্ণৰূপে দ্ৰৱণীয়; ৫-৮% দ্ৰৱণক ভিনেগাৰ হিচাপে ব্যৱহাৰ কৰা হয়। |
| গলনাংক | গলনাংক নিম্ন (-114°C), সাধাৰণ তাপমাত্ৰাত তৰল অৱস্থাত থাকে। | গলনাংক ১৬.৬°C (২৯০ K), শীতকালত গোটমাৰে। |
| ঘনত্ব | পানীতকৈ ঘনত্ব কম (0.789 g/cm³)। | পানীতকৈ ঘনত্ব বেছি (1.049 g/cm³), সেয়েহে পানীৰ তলত জমা হয়। |
ৰাসায়নিক ধৰ্ম:
| ইথানল (C₂H₅OH) | ইথানয়িক এচিড (CH₃COOH) | |
|---|---|---|
| ছডিয়ামৰ সৈতে বিক্ৰিয়া | ছডিয়াম ধাতুৰ সৈতে বিক্ৰিয়া কৰি হাইড্ৰ’জেন গেছ আৰু ছডিয়াম ইথক্সাইড উৎপন্ন কৰে। সমীকৰণ: 2C₂H₅OH + 2Na → 2C₂H₅ONa + H₂ |
ছডিয়ামৰ সৈতে বিক্ৰিয়া নকৰে, কাৰণ ইয়াৰ এলক’হলৰ দৰে হাইড্ৰ’ক্সিল গ্ৰুপ নাথাকে। |
| ছডিয়াম বাইকাৰ্বনেটৰ সৈতে বিক্ৰিয়া | কোনো বিক্ৰিয়া নকৰে, কাৰণ ইথানল এচিড নহয়। | ছডিয়াম বাইকাৰ্বনেটৰ সৈতে বিক্ৰিয়া কৰি কাৰ্বন ডাই অক্সাইড গেছ, পানী আৰু ছডিয়াম এচিটেট উৎপন্ন কৰে। সমীকৰণ: CH₃COOH + NaHCO₃ → CH₃COONa + H₂O + CO₂ |
| নিৰুদন (ডিহাইড্ৰেচন) | গাঢ় H₂SO₄ৰ উপস্থিতিত উত্তপ্ত কৰিলে পানী হেৰুৱাই ইথিন (C₂H₄) উৎপন্ন কৰে। সমীকৰণ: C₂H₅OH → C₂H₄ + H₂O |
নিৰুদন নহয়, কাৰণ ইথানয়িক এচিডত ইথানলৰ দৰে হাইড্ৰ’ক্সিল গ্ৰুপ নাথাকে। |
| এষ্টাৰিভৱন | ইথানয়িক এচিডৰ সৈতে বিক্ৰিয়া কৰি এষ্টাৰ (ইথাইল এচিটেট) গঠন কৰে। সমীকৰণ: C₂H₅OH + CH₃COOH → CH₃COOC₂H₅ + H₂O |
এলক’হলৰ (যেনে, ইথানল) সৈতে গাঢ় H₂SO₄ৰ উপস্থিতিত বিক্ৰিয়া কৰি এষ্টাৰ গঠন কৰে। সমীকৰণ: CH₃COOH + C₂H₅OH → CH₃COOC₂H₅ + H₂O |
উত্তৰ:
পানীত ফেন উঠাৰ কাৰণ:
চাবোন অণুৰ দুটা অংশ থাকে এটা জলাকৰ্ষী মূৰ (-COO⁻Na⁺) আৰু আনটো জলবিকৰ্ষী পুচ্ছ (দীঘল হাইড্ৰ’কাৰ্বন শৃংখল)। পানীত চাবোনে মাইছেল গঠন কৰে, য’ত জলবিকৰ্ষী পুচ্ছ মলিৰ চাৰিওফালে জমা হয় আৰু জলাকৰ্ষী মূৰ পানীৰ সৈতে সংযুক্ত হৈ থাকে। ঘোটালি দিলে এই মাইছেলবোৰ বায়ুৰ বুদবুদৰ সৈতে মিহলি হৈ ফেন উৎপন্ন কৰে।
ইথানলত ফেন উঠে নে?:
ইথানলত ফেন নুঠে। কাৰণ ইথানল জৈৱ দ্ৰৱক। ইথান'লত চাবোনৰ জলাকৰ্ষী আৰু জলবিকৰ্ষী অংশৰ মাজত পাৰ্থক্যৰ প্ৰভাৱ কম হয়। ফলত মাইছেল গঠন নহয়, আৰু ফেন উৎপন্ন নহয়।
উত্তৰ: কাৰ্বন আৰু ইয়াৰ যৌগ (যেনে মিথেন, ইথানল, পেট্ৰ’ল) ইন্ধন হিচাপে ব্যৱহাৰ হয় কাৰণ:
- ইহঁতৰ দহনত উচ্চ তাপ উৎপন্ন হয়। যেতিয়া কাৰ্বন যৌগ অক্সিজেনৰ উপস্থিতিত দহন কৰা হয় তেতিয়া কাৰ্বন ডাই অক্সাইড আৰু পানী উৎপন্ন কৰি প্ৰচুৰ তাপ শক্তি মুক্ত কৰে।
- ইয়াৰোপৰিও কাৰ্বন যৌগ যেনে কয়লা, পেট্ৰলিয়াম, আৰু প্ৰাকৃতিক গেছ পৃথিৱীত প্ৰচুৰ পৰিমাণে পোৱা যায়।
- এই যৌগবোৰ সহজে জ্বলে আৰু শক্তি উৎপন্ন কৰে।
- কাৰ্বন যৌগৰ বিভিন্ন ৰূপ (তৰল, গেছ, কঠিন) বিভিন্ন কামৰ বাবে উপযোগী।
উদাহৰণ: CH₄ + 2O₂ → CO₂ + 2H₂O + তাপ
উত্তৰ: কঠিন পানীত কেলছিয়াম (Ca²⁺) আৰু মেগনেছিয়াম (Mg²⁺) আয়ন থাকে। চাবোনে (RCOONa) এই আয়নৰ সৈতে বিক্ৰিয়া কৰি অদ্ৰৱণীয় কেলছিয়াম বা মেগনেছিয়াম লৱণ গঠন কৰে, যাক গেদ বোলে।
বিক্ৰিয়া:
2RCOONa + Ca²⁺ → (RCOO)₂Ca + 2Na⁺
[(RCOO)₂Ca হ’ল অদ্ৰৱণীয় গেদ]
এই গেদ পানীত জমা হৈ ফেন গঠনত বাধা দিয়ে আৰু কাপোৰত লাগি থাকিব পাৰে।
উত্তৰ: চাবোন (RCOONa) হৈছে ক্ষাৰকীয় পদাৰ্থ কাৰণ ই কাৰ্বক্সিলিক এচিডৰ লৱণ।
নীলা লিটমাছ কাগজ: কোনো পৰিৱৰ্তন নহ’ব, কাৰণ চাবোন আম্লিক নহয়।
ৰঙা লিটমাছ কাগজ: ৰঙা লিটমাছ নীলা হৈ পৰিব, কাৰণ চাবোনৰ ক্ষাৰকীয় ধৰ্মৰ বাবে ই লিটমাছৰ ৰং সলনি কৰে।
উত্তৰ: অসংপৃক্ত হাইড্ৰ’কাৰ্বনৰ সৈতে নিকেল বা পেলাডিয়াম অনুঘটকৰ উপস্থিতিত হাইড্ৰ’জেন যোগ কৰি সংপৃক্ত হাইড্ৰ’কাৰ্বনলৈ ৰূপান্তৰ কৰা প্ৰক্ৰিয়াক হাইড্ৰ’জেনেচন বোলে।
উদাহৰণ:
CH₂=CH₂ + H₂ → CH₃-CH₃ (Pd/Ni অনুঘটকৰ উপস্থিতিত)
ঔদ্যোগিক প্ৰয়োগ:
- বনস্পতি ঘি উৎপাদন: উদ্ভিদজাত তেল (অসংপৃক্ত)ক হাইড্ৰ’জেনেচনৰ জৰিয়তে বনস্পতি ঘি (সংপৃক্ত)লৈ ৰূপান্তৰ কৰা হয়।
- পেট্ৰ’লিয়াম শোধন: অসংপৃক্ত হাইড্ৰ’কাৰ্বনক সংপৃক্ত কৰি উন্নত ইন্ধন তৈয়াৰ কৰা হয়।
C₂H₂, C₃H₈, C₃H₆, C₂H₆, CH₄
উত্তৰ: যোগাত্মক বিক্ৰিয়া অসংপৃক্ত হাইড্ৰ’কাৰ্বন (এলকিন আৰু এলকাইন) এ দেখুৱায়।
- C₂H₂ (ইথাইন): এলকাইন, ত্ৰি-বান্ধনি আছে। যোগাত্মক বিক্ৰিয়া দেখুৱায়।
- C₃H₈ (প্ৰ’পেন): এলকেন, এক বান্ধনি আছে। যোগাত্মক বিক্ৰিয়া নকৰে।
- C₃H₆ (প্ৰ’পিন): এলকিন, দ্বি-বান্ধনি আছে। যোগাত্মক বিক্ৰিয়া দেখুৱায়।
- C₂H₆ (ইথেন): এলকেন, এক বান্ধনি আছে। যোগাত্মক বিক্ৰিয়া নকৰে।
- CH₄ (মিথেন): এলকেন, এক বান্ধনি আছে। যোগাত্মক বিক্ৰিয়া নকৰে।
C₂H₂ আৰু C₃H₆ এ যোগাত্মক বিক্ৰিয়া দেখুৱায়।
উত্তৰ: মাখনত সংপৃক্ত চৰ্বি আৰু খোৱা তেলত অসংপৃক্ত চৰ্বি পোৱা যায়। এই পাৰ্থক্য দেখুৱাবলৈ তলত দিয়া পৰীক্ষাটো কৰা হয়:
ব্ৰ’মিন পানী পৰীক্ষা:
পদ্ধতি: দুটা পৰীক্ষা নলীত ক্ৰমে মাখন আৰু খোৱা তেল লৈ তাত কেইটোপালমান ব্ৰ’মিন পানী (কমলা ৰঙৰ) যোগ কৰা হ'ল।
পৰ্যবেক্ষণ:
- খোৱা তেলৰ নলীত ব্ৰ’মিন পানীৰ কমলা ৰং নোহোৱা হৈ যাব, কাৰণ অসংপৃক্ত চৰ্বিয়ে ব্ৰ’মিনৰ সৈতে যোগাত্মক বিক্ৰিয়া কৰি বৰণহীন হৈ পৰে।
- মাখনৰ নলীত ব্ৰ’মিন পানীৰ কমলা ৰং থাকিব, কাৰণ সংপৃক্ত চৰ্বিয়ে ব্ৰ'মিণৰ সৈতে যোগাত্মক বিক্ৰিয়া নকৰে।
ব্যাখ্যা: অসংপৃক্ত যৌগত দ্বি- বা ত্ৰি-বান্ধনি থাকে, যিয়ে ব্ৰ’মিণৰ সৈতে বিক্ৰিয়া সংঘটিত কৰে।
উত্তৰ:
চাবোনৰ মলি আঁতৰোৱাৰ প্ৰক্ৰিয়া মাইছেল গঠনৰ ওপৰত নিৰ্ভৰ কৰে।
চাবোনৰ গঠন: চাবোনৰ অণুত দুটা অংশ:
- জলাকৰ্ষী মূৰ (-COO⁻Na⁺): যিটো পানীত দ্ৰৱণীয়
- জলবিকৰ্ষী পুচ্ছ (দীঘল হাইড্ৰ'কাৰ্বন শৃংখল): যিটো তেল বা মলিত দ্ৰৱণীয়
পানীত চাবোন অণুবোৰে গোলাকাৰ মাইছেল গঠন কৰে। জলবিকৰ্ষী পুচ্ছবোৰ মলি বা তেলৰ টোপালৰ ফালে আকৰ্ষিত হয়, আৰু জলাকৰ্ষী মূৰবোৰ পানীৰ সৈতে সংযুক্ত হৈ থাকে।
যেতিয়া চাবোন মিহলি কাপোৰ ঠেকেচি দিয়া হয় মাইছেলবোৰে মলিৰ টোপালক ঘেৰি ধৰে আৰু ইমালছন গঠন কৰে। এই ইমালছন পানীৰ সৈতে ধুই পেলালে কাপোৰৰ পৰা মলি আঁতৰি পৰিষ্কাৰ হৈ পৰে।